Las mitocondrias han sido reconocidas clásicamente como los orgánulos encargados de la producción de energía en forma de ATP. El proceso de biogénesis mitocondrial, que implica la formación de nuevas mitocondrias a partir de las ya existentes, es fundamental para mantener una buena salud, prevenir enfermedades crónicas y optimizar el rendimiento deportivo.
Tabla de contenidos
¿Qué son las mitocondrias?
Las mitocondrias son orgánulos celulares fundamentales que actúan como las centrales energéticas del cuerpo. Su función principal es convertir los nutrientes en energía utilizable en forma de ATP, el combustible esencial para la contracción muscular y otras funciones biológicas.
La eficiencia y cantidad de mitocondrias en el músculo determinan en gran medida la capacidad aeróbica y la oxidación de grasas durante el ejercicio.
Su capacidad funcional depende del número, tamaño y eficiencia de estas estructuras, lo cual puede modificarse mediante estímulos fisiológicos como el ejercicio o intervenciones dietéticas (Hood, 2009).
¿Por qué son importantes?
Las mitocondrias son responsables de la fosforilación oxidativa o beta-oxidación de los ácidos grasos, produciendo hasta el 90% del ATP celular a través del ciclo de Krebs y la cadena de transporte de electrones. Este proceso es crucial en la “quema de grasa”, por eso, cuantas más mitocondrias tengan las células, mayor será su capacidad para oxidar ácidos grasos y producir energía, lo que incrementa la capacidad del organismo para utilizar grasas como combustible.
En el interior de las mitocondrias, ancladas en la membrana interna, encontramos verdaderas nanomáquinas moleculares como la ATP sintasa, responsable de transformar el gradiente de protones generado durante la oxidación de nutrientes en ATP, la moneda energética del organismo.
Esta proteína trabaja como un motor rotatorio: gira, se mueve y produce energía de forma continua, siempre que disponga de sustratos adecuados (oxígeno, ácidos grasos, glucosa) y de una mitocondria estructuralmente sana.
Cuanto más eficiente es esta maquinaria, mayor es nuestra capacidad para:
- generar ATP durante el ejercicio,
- sostener esfuerzos prolongados,
- utilizar grasa como combustible,
- y mantener la estabilidad metabólica en reposo.
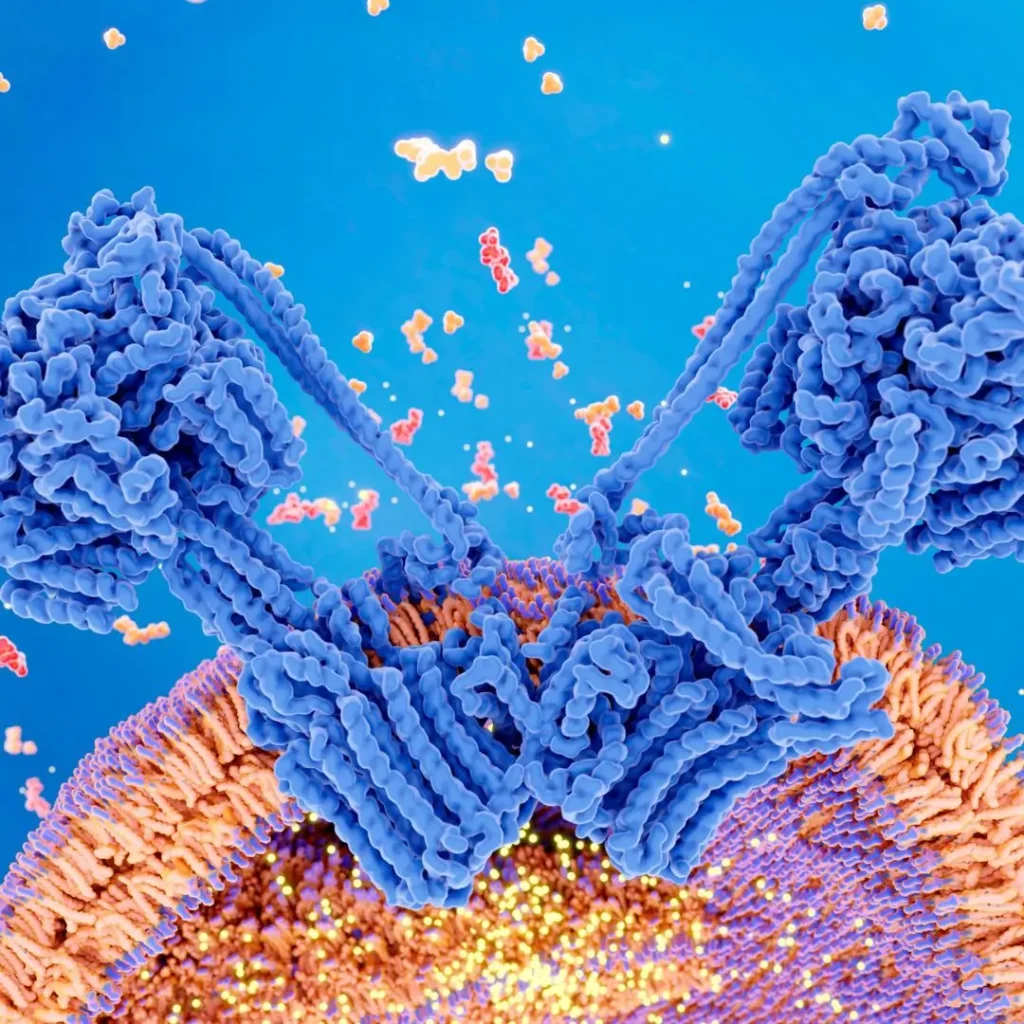
“La ATP sintasa produce la energía que usará el músculo, el cerebro y todos los tejidos”
Si quieres profundizar más sobre la fisiología que hay detrás de la pérdida de grasa puedes leer el siguiente artículo:
- Fisiología de la pérdida de grasaFisiología de la pérdida de grasa
Además, participan en la homeostasis del calcio, la apoptosis, la generación de especies reactivas de oxígeno (ROS) y la señalización metabólica. Investigaciones recientes revelan que su función trasciende la bioenergética, participando en procesos esenciales como la regulación del metabolismo, la inflamación, el envejecimiento y el rendimiento físico (Hamilpur et al., 2025).
“El cerebro es uno de los órganos que más energía consume”
Biogénesis mitocondrial
La biogénesis mitocondrial es el proceso por el cual se incrementa la masa y número de mitocondrias dentro de las células, mediado por factores nucleares y mitocondriales que coordinan la expresión génica dual.
Uno de los principales reguladores es PGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha), que actúa como coactivador de factores de transcripción como NRF1 y NRF2, estimulando genes que controlan la replicación del ADN mitocondrial y la síntesis de proteínas mitocondriales (Wu et al., 1999).
“Las mitocondrias son altamente moldeables y se reproducen ellas mismas”
La biogénesis mitocondrial no solo incrementa el número de mitocondrias, sino que optimiza la arquitectura interna, favoreciendo la formación de más crestas mitocondriales y una mayor densidad de ATP sintasas. Esto se traduce en una mayor capacidad oxidativa y una mejor respuesta frente a demandas energéticas elevadas
Señales que activan la biogénesis mitocondrial
Las siguientes señales convergen en rutas que promueven una mayor capacidad oxidativa y resistencia celular al estrés (Puigserver & Spiegelman, 2003). Esto es importante para potenciar tus mitocondrias
Los ritmos circadianos y la luz
La biogénesis mitocondrial está intrínsecamente ligada a la homeostasis circadiana. Evidencias recientes revelan que los ritmos circadianos —regulados principalmente por señales lumínicas naturales— ejercen un papel central en la activación de factores de transcripción claves como PGC-1α, NRF-1 y TFAM, moduladores directos de la replicación mitocondrial (Andrews et al. 2010; Gerhart-Hines et al., 2011)
Los ritmos circadianos son oscilaciones de ~24 h que regulan procesos celulares, incluyendo el metabolismo, mediante relojes moleculares como CLOCK y BMAL1. Estas proteínas controlan genes implicados en la función mitocondrial. La biogénesis mitocondrial, por su parte, permite a las células aumentar su número de mitocondrias ante demandas energéticas o estrés oxidativo.
Los factores que sincronizan el reloj circadiano, especialmente la luz natural, influyen en cascadas metabólicas esenciales. Puedes profundizar más al respecto en el siguiente enlace:
- Cómo la luz afecta al ritmo circadianoNuevoCómo la luz afecta al ritmo circadiano
El ejercicio fisico
El ejercicio físico, especialmente el ejercicio aeróbico y el entrenamiento de resistencia, es un modulador significativo en la biogénesis mitocondrial. Induce la activación de varios factores que favorecen la biogénesis mitocondrial al incrementar la expresión de proteína PGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha), que es clave para el aumento del número y la función de las mitocondrias, a través de la activación de AMPK y p38 MAPK.
Ejercicio aeróbico: Actividades como correr, nadar o andar en bicicleta, realizadas a una intensidad moderada y por periodos prolongados, son altamente eficaces en la estimulación de la biogénesis mitocondrial. Esto es porque el ejercicio aeróbico prolongado demanda un mayor uso de ácidos grasos como fuente de energía, lo que provoca adaptaciones celulares, como el aumento en el número de mitocondrias, para satisfacer esas demandas energéticas.
Entrenamiento de resistencia: Aunque se suele asociar el ejercicio aeróbico con el aumento de mitocondrias, los entrenamientos de resistencia también contribuyen a la mejora de la capacidad mitocondrial, ya que promueven la utilización de ácidos grasos como fuente de energía para los músculos durante periodos prolongados de esfuerzo.
La restricción calórica o el ayuno
La restricción calórica (sin malnutrición) ha sido vinculada con la activación de vías que favorecen la biogénesis mitocondrial, aumentando la capacidad del cuerpo para producir nuevas mitocondrias. Esto se debe a la activación de reguladores metabólicos como AMPK y SIRT1, que también están involucrados en la respuesta al ejercicio. Estos reguladores activan la proteína PGC-1α, lo que promueve la formación de mitocondrias y mejora la función mitocondrial.
Relación de la biogénesis mitocondrial con la salud metabólica
Un bajo número o funcionalidad mitocondrial se asocia con enfermedades como obesidad, diabetes tipo 2 y síndrome metabólico (Patti et al., 2003). La estimulación de la biogénesis mitocondrial mejora la sensibilidad a la insulina y la oxidación de lípidos.
Lactato como reflejo de la salud mitocondrial
Durante décadas, el lactato fue considerado un simple residuo metabólico, responsable de la fatiga muscular. Hoy, investigaciones como la de Zhang et al. (2024) han demostrado que el lactato se reconoce como combustible como una molécula señalizadora clave que estimula la biogénesis mitocondrial y optimiza el metabolismo energético.
Al elevarse durante el ejercicio intenso, el lactato activa rutas de comunicación celular – mediadas por transportadores como MCT1 – que impulsan la adaptación oxidativa del músculo y el acoplamiento mitocondrial, mejorando la eficiencia del ciclo del ácido tricarboxílico (TCA) y la capacidad de producción de energía. Esto apoya el papel del lactato como regulador clave de la función energética celular y como una molécula señalizadora que modula la biogénesis mitocondrial, y por tanto, mejora de la capacidad oxidativa (Storoschuk et al., 2025; Zhang et al., 2024).
En un músculo sano con mitocondrias funcionales, el lactato es reciclado eficientemente en el ciclo de Cori o convertido en piruvato para ingresar a la mitocondria y ser oxidado. Sin embargo, cuando hay disfunción mitocondrial, este procesamiento se ve comprometido, lo que resulta en una acumulación de lactato en sangre incluso a bajos niveles de esfuerzo físico. Así, el lactato elevado se convierte en un marcador indirecto de un metabolismo energético ineficiente (Storoschuk et al., 2025)
Este principio encarna el fenómeno conocido como mitohormesis: la idea de que una dosis controlada de estrés metabólico (como el generado por el ejercicio intenso o el incremento de lactato) estimula mecanismos celulares de supercompensación y resiliencia.
Mitohormesis
La mitohormesis es un concepto biológico donde un estrés leve y temporal en las mitocondrias desencadena una respuesta adaptativa que mejora la función mitocondrial y la salud celular, activando vías de defensa, reparando disfunciones y aumentando la resistencia a estrés futuro (Cheng et al., 2023)
Las mitocondrias generan niveles bajos del ROS, que a su vez actúan como moléculas de la transmisión de señales y protegen las células contra daño adicional iniciando una reacción adaptante (mecanismo de defensa de la tensión).
Es una forma de hormesis (beneficios por dosis bajas de estrés) enfocada en las mitocondrias, promoviendo la comunicación entre ellas y el núcleo celular para un mejor equilibrio (homeostasis)
“No se trata de evitar el estrés, sino de aplicarlo en dosis saludables, así un pequeño daño puede ser una señal para que la célula se fortalezca”
Factores que promueven la biogénesis mitocondrial
El ejercicio físico
Según Türket y colaboradores (2022) el ejercicio actúa como un potente desencadenante de respuestas mitohorméticas, promoviendo una renovación mitocondrial que mejora la salud metabólica, cardiovascular y neurológica. Tanto el entrenamiento de resistencia en zona 2 (aeróbico) como el entrenamiento de alta intensidad (HIIT) elevan la biogénesis mitocondrial al provocan un aumento de PGC-1α y citocromo c (Little et al., 2011).
Estudios como el de Pearson et al. (2023) muestran que el entrenamiento de alta intensidad induce mejoras en la función mitocondrial y vascular, al exponer al cuerpo a picos de estrés que generan altas concentraciones de lactato y radicales libres mitocondriales (mtROS), evidenciando que el dolor controlado y el esfuerzo máximo no son destructivos, sino catalizadores de adaptación fisiológica.
No obstante, si queremos estimular al máximo las mitocondrias con ejercicio, nada mejor que entrenar en la llamada “zona 2”, el rango de entrenamiento aeróbico moderado, que correspondiente a un 60-70% de la frecuencia cardíaca máxima, donde predomina la oxidación de grasas como fuente principal de energía. Entrenar en este rango promueve la densidad mitocondrial, la capacidad oxidativa del músculo y la eficiencia metabólica general (Storoschuk et al., 2025)
Si quieres profundizar en la frecuencia cardíaca y aprender a calcular las zonas de frecuencia cardíaca, te recomiendo leer el siguiente artículo:
- Zonas de frecuencia cardíacaZonas de frecuencia cardíaca
Paradójicamente, el “dolor” metabólico del entrenamiento intenso es el lenguaje con el que las mitocondrias aprenden a resistir. Si se dosifica adecuadamente —sin caer en el sobreentrenamiento—, el estrés oxidativo y el lactato actúan como señales que refuerzan la capacidad del organismo para producir energía, recuperarse más rápido y volverse más eficiente.
“El clásico dogma del “no pain, no gain” adquiere un nuevo significado: no se trata de sufrir más tiempo, sino de estimular mejor, en las dosis justas”
El ayuno intermitente
Estimula la autofagia mitocondrial (mitofagia) y activa vías AMPK y SIRT1 y mejora la salud metabólica y mitocondrial [Longo & Panda, 2016].

Puedes profundizar en el conocimiento del ayuno a través de los siguientes enlaces:
- Ayuno intermitente: tipos de ayuno y beneficiosAyuno intermitente: tipos de ayuno y beneficios
- Fisiología del ayuno: ¿Qué ocurre en el cuerpo?Fisiología del ayuno: ¿Qué ocurre en el cuerpo?
Intervenciones dietéticas
La dieta cetogénica
La dieta cetogénica eleva la biogénesis mitocondrial por aumento de cuerpos cetónicos que activan PGC-1α. Las dietas altas en grasas y bajas en carbohidratos, como la dieta cetogénica, han demostrado promover la biogénesis mitocondrial. Los cuerpos cetónicos —principalmente β-hidroxibutirato— actúan como moléculas señalizadoras que estimulan la expresión de PGC-1α y SIRT3, mejorando la función mitocondrial y reduciendo el estrés oxidativo (Newman & Verdin, 2013)
Además, el cambio en el metabolismo energético favorece la utilización de ácidos grasos, lo cual exige una mayor capacidad oxidativa y adaptaciones mitocondriales.
Si quieres aprender más sobre la dieta cetogénica y la cetosis nutricional, puedes leer los siguientes enlaces:
- La dieta cetogénicaLa dieta cetogénica
- Cetosis: Un estado metabólico ancestralCetosis: Un estado metabólico ancestral
La exposición al frío
La exposición a temperaturas frías ha sido relacionada con el aumento de la actividad de la grasa parda, un tipo de tejido adiposo que contiene muchas mitocondrias. La grasa parda es un tejido rico en mitocondrias y altamente especializado en la producción de calor (termogénesis) a través de la proteína desacoplante UCP1. La exposición al frío activa esta grasa, lo que conlleva un aumento en la biogénesis mitocondrial, particularmente en personas adaptadas al frío o en prácticas como la crioterapia.
El frío también induce la expresión de PGC-1α y genes relacionados con la función mitocondrial en el tejido adiposo
El frío activa las mitocondrias en la grasa parda para generar calor, un proceso conocido como termogénesis sin escalofríos.
Terapia de luz roja
La terapia de luz roja consiste en la exposición a longitudes de onda específicas de luz roja (600–700 nm) o infrarroja cercana (700–1000 nm), que penetran tejidos biológicos y modulan la actividad celular, especialmente la función mitocondrial.
La luz roja se ha observado que estimula directamente el complejo IV de la cadena de transporte de electrones, lo que mejora el uso del oxígeno, aumenta la producción de ATP (energía celular) y disminuye el estrés oxidativo (Rojas et al., 2011)
Además, la terapia de luz roja se asocia con una reducción de la inflamación crónica (un factor que deteriora las mitocondrias). Si quieres profundizar sobre la terapia de luz roja te dejo el siguiente enlace:
- Terapia de luz rojaNuevoTerapia de luz roja

Suplementación
Resveratrol
Un compuesto encontrado en la piel de las uvas, ha mostrado en estudios de laboratorio la capacidad de activar SIRT1, lo que podría promover la biogénesis mitocondrial al promover PGC-1α.
Magnesio
El magnesio es un cofactor esencial para más de 300 reacciones enzimáticas, muchas de ellas mitocondriales. Participa en la síntesis de ATP, el transporte de electrones, y la estabilización del ADN mitocondrial.
Una deficiencia de magnesio reduce la eficiencia mitocondrial, aumenta el estrés oxidativo y está relacionada con disfunción muscular y fatiga crónica. Su suplementación se asocia con mejoras en la eficiencia energética celular y mayor tolerancia al ejercicio (Nielsen, 2010)
¿Por qué sería interesante suplementar con magnesio por encima de otros complementos alimenticios?
Si los niveles de magnesio no se restauran y se mantienen bajos facilitan el desarrollo de enfermedades relacionadas con el envejecimiento, como la osteoporosis.
El magnesio es el único mineral que tiene hasta una revista de investigación, Magnesium Research, es sin duda fundamental para que funcionen las enzimas del cuerpo, un suplemento de cabecera y seguro.
¿Cuál sería una dosis recomendada?
Se puede suplementar entre 300 y 600 mg al día
Puedes consultar algunos suplementos de magnesio en el siguiente enlace:
- Suplementos de magnesio: todo lo que necesitas saberSuplementos de magnesio: todo lo que necesitas saber
Coenzima Q10
Este suplemento es un antioxidante que se encuentra naturalmente en las mitocondrias y juega un papel en la cadena de transporte de electrones. Se ha sugerido que puede mejorar la función mitocondrial y estimular la biogénesis, aunque los resultados no siempre son consistentes. Mejora la función mitocondrial en enfermedades cardiovasculares.
PQQ (pirroloquinolina quinona):
Potente activador de la biogénesis.
Creatina
La creatina favorece indirectamente la biogénesis mitocondrial a través del aumento de la disponibilidad de ATP y la activación de vías metabólicas reguladoras. Estudios preclínicos han demostrado que CrM, combinada con ejercicio de resistencia, estimula la expresión de PGC-1α (Taskin et al., 2022; Marshall et al., 2022). Esta activación favorece la síntesis de nuevas mitocondrias, mejorando la eficiencia metabólica del músculo y la tolerancia al ejercicio.
Además, creatina puede reducir el estrés oxidativo mitocondrial y modular genes implicados en la dinámica mitocondrial (fusión y fisión), lo que contribuye a una red mitocondrial más saludable en células musculares (Sestili et al., 2016).
En el cerebro, la creatina cumple funciones bioenergéticas similares, al servir como reservorio de fosfatos para la rápida regeneración de ATP. Dado que el cerebro es altamente dependiente de energía, una mayor disponibilidad de creatina puede facilitar funciones cognitivas complejas.
Evidencia en humanos y modelos animales sugiere que la suplementación con CrM puede mejorar la memoria de trabajo, la atención y el aprendizaje espacial, al potenciar la bioenergía cerebral y regular procesos mitocondriales (Snow et al., 2018; Jivan, 2024). A nivel molecular, se ha observado una mayor expresión de proteínas mitocondriales y antioxidantes en el hipocampo tras suplementación prolongada.
Además, en adultos mayores, la creatina monohidrato ha mostrado efectos neuroprotectores, atenuando procesos neurodegenerativos al sostener la función mitocondrial y reducir especies reactivas de oxígeno (Forbes et al., 2022).
Si quieres profundizar más sobre la creatina monohidrato y conocer las mejores recomendaciones, puedes hacer clic en el siguiente enlace:
- Creatina MonohidratoCreatina Monohidrato
Ácido alfa lipoico
El ácido alfa lipoico estimula la oxidación de ácidos grasos cuando hay una baja presencia de hidratos de carbono en la dieta.
Genética y epigenética de la función mitocondrial
“La genética juega un papel crucial tanto en el número como en la función mitocondrial”
La capacidad de aumentar el número de mitocondrias depende también de la genética y los factores epigenéticos que influyen en la biogénesis y la función mitocondrial. La función mitocondrial está codificada por genes tanto del genoma nuclear como del ADN mitocondrial (mtDNA). Variaciones genéticas pueden afectar la eficiencia de la fosforilación oxidativa, la producción de ROS y la capacidad de adaptación al ejercicio (Latorre-Pellicer et al., 2016)
Además, mecanismos epigenéticos (metilación del ADN, acetilación de histonas, miARNs) regulan la expresión de genes relacionados con la biogénesis mitocondrial, especialmente bajo condiciones de estrés o envejecimiento. La activación de SIRT1 y SIRT3, asociada con restricción calórica o ejercicio, modifica la expresión génica mitocondrial a través de la desacetilación de PGC-1α [Kelly & Scarpulla, 2004].
Las mitocondrias tienen su propio ADN mitocondrial (ADNmt), que es heredado exclusivamente de la madre. Este ADN mitocondrial codifica algunas de las proteínas necesarias para la función mitocondrial, aunque la mayoría de los genes involucrados en la biogénesis mitocondrial se encuentran en el núcleo celular.
Variaciones genéticas
Las variaciones en el ADN mitocondrial pueden afectar la eficiencia con la que las mitocondrias producen energía. Algunos estudios han demostrado que ciertas mutaciones en el ADNmt están asociadas con enfermedades mitocondriales que afectan la producción de ATP y el metabolismo energético, lo que puede tener un impacto negativo en la quema de grasa y en la energía disponible.
Regulación genética nuclear
Los genes ubicados en el núcleo que regulan la biogénesis mitocondrial, como el gen que codifica para PGC-1α, están bajo control de factores genéticos y ambientales. Las personas con variantes genéticas favorables en estos genes pueden tener una mayor capacidad para aumentar la cantidad de mitocondrias y mejorar su función en respuesta al ejercicio o a otros estímulos.
Herencia materna
¿Sabías que el ADN mitocondrial se hereda exclusivamente de la madre?
Como el ADN mitocondrial se hereda exclusivamente de la madre, las mutaciones o variaciones en el ADNmt pueden ser transmitidas de generación en generación. Las deficiencias o mutaciones en el ADNmt pueden afectar la capacidad del individuo para producir suficiente energía a partir de las mitocondrias, lo que podría influir en la capacidad para quemar grasas de manera eficiente.
Epigenética
La epigenética también influye en la función mitocondrial. Cambios epigenéticos, como la metilación del ADN y modificaciones de histonas, pueden regular la expresión de genes involucrados en la biogénesis mitocondrial, alterando así el número y la funcionalidad de las mitocondrias. Estos cambios pueden ser inducidos por el entorno, como la dieta, el ejercicio o el estrés oxidativo.
Envejecimiento y disfunción mitocondrial
El envejecimiento se asocia con una disminución progresiva de la función mitocondrial, aumento de ROS y mutaciones en el ADN mitocondrial (mtDNA). Estos cambios promueven inflamación crónica, pérdida de masa muscular (sarcopenia) y fragilidad (Bratic & Larsson, 2013).
Una de las señales más comunes del deterioro mitocondrial es la fatiga constante. La disfunción mitocondrial está relacionada con enfermedades como enfermedades neurodegenerativas como el Alzheimer o el Parkinson, también con la diabetes tipo 2 y la obesidad.
La biogénesis mitocondrial contrarresta estos efectos mediante la renovación mitocondrial y mejora del metabolismo energético. Optimizar las mitocondrias mejora la memoria, la concentración y reduce el riesgo de enfermedades neurodegenerativas.
“Mejorar el rendimiento mitocondrial puede aumentar significativamente la energía vital diaria”
Disfunción mitocondrial: piedra angular de enfermedades crónicas
La disfunción mitocondrial es un denominador común en diversas enfermedades crónicas no transmisibles, desde la resistencia a la insulina hasta el cáncer. En condiciones fisiológicas normales, las mitocondrias regulan la producción de energía (ATP) a través de la fosforilación oxidativa. Sin embargo, cuando este sistema falla, se desencadena un desbalance metabólico sistémico que afecta a tejidos de alta demanda energética como el músculo esquelético, el hígado y el cerebro.
La resistencia a la insulina, por ejemplo, se asocia con una disminución en la capacidad mitocondrial para oxidar ácidos grasos, lo que promueve la acumulación de lípidos en tejidos no adiposos y genera estrés oxidativo (Kim et al., 2025).
Asimismo, en diversos tipos de cáncer, las células recurren a vías metabólicas alternativas, como la glucólisis aeróbica (efecto Warburg), precisamente porque la función mitocondrial está alterada, lo cual favorece su crecimiento descontrolado (Barbosa et al., 2025).
La evidencia acumulada sugiere que la pérdida de eficiencia mitocondrial precede y perpetúa el estado inflamatorio crónico y la disfunción energética que caracteriza muchas enfermedades modernas, incluido el autismo o el trastorno por déficit de atención e hiperactividad (Yang et al., 2026).
Conclusiones
La biogénesis mitocondrial representa un puente entre el metabolismo celular, el rendimiento físico y la salud a largo plazo. Su regulación ofrece oportunidades terapéuticas y preventivas en campos como la medicina deportiva, el envejecimiento saludable y la rehabilitación.
Estimular la biogénesis mitocondrial mediante estilos de vida activos, alimentación y suplementos adecuados, puede ser una de las estrategias más efectivas para mejorar la calidad de vida.
El ejercicio físico, la restricción calórica, la dieta cetogénica, ciertos suplementos, y la exposición al frío pueden estimular la biogénesis mitocondrial.
La genética influye en la eficiencia de las mitocondrias, tanto a nivel del ADN mitocondrial como de los genes nucleares que regulan su producción.
La epigenética juega un papel regulador en la expresión de genes relacionados con la biogénesis mitocondrial, lo que permite que el entorno modifique la capacidad del cuerpo para aumentar el número de mitocondrias.
La combinación de ejercicio, ayuno intermitente y suplementación controlada forma parte de estrategias integrativas de medicina funcional.
Referencias
Andrews JL, Zhang X, McCarthy JJ, McDearmon EL, Hornberger TA, Russell B, Campbell KS, Arbogast S, Reid MB, Walker JR, Hogenesch JB, Takahashi JS, Esser KA. CLOCK and BMAL1 regulate MyoD and are necessary for maintenance of skeletal muscle phenotype and function. Proc Natl Acad Sci U S A. 2010 Nov 2;107(44):19090-5. doi: 10.1073/pnas.1014523107. Epub 2010 Oct 18. PMID: 20956306; PMCID: PMC2973897. [PubMed]
Barbosa, F., Cunha, A., Barbosa, J., et al. (2025). The Dual Role of Metformin: Repurposing an Antidiabetic Drug for Cancer Therapy. Applied Sciences, 15(21), 11576. [MDPI]
Bratic, A., & Larsson, N.G. (2013). The role of mitochondria in aging. J Clin Invest, 123(3), 951–957. [Enlace]
Cannon, B., & Nedergaard, J. (2004). Brown adipose tissue: function and physiological significance. Physiological Reviews, 84(1), 277–359. [Enlace]
Cheng, Y. W., Liu, J., & Finkel, T. (2023). Mitohormesis. Cell Metabolism, 35(10), 1659–1676. [Cell]
Forbes, S. C., Candow, D. G., & Ferreira, L. H. B. (2022). Effects of creatine on muscle, bone, and brain. Current Issues in Molecular Biology, 44(1), 322–342. [PubMed]
Hamilpur, A.B., et al. (2025). Applying Longevity and Anti-Aging Research to Athletic Performance. IJSSeR. PDF
Hood DA. Mechanisms of exercise-induced mitochondrial biogenesis in skeletal muscle. Appl Physiol Nutr Metab. 2009 Jun;34(3):465-72. doi: 10.1139/H09-045. PMID: 19448716. [PubMed]
Gerhart-Hines Z, Dominy JE Jr, Blättler SM, Jedrychowski MP, Banks AS, Lim JH, Chim H, Gygi SP, Puigserver P. The cAMP/PKA pathway rapidly activates SIRT1 to promote fatty acid oxidation independently of changes in NAD(+). Mol Cell. 2011 Dec 23;44(6):851-63. doi: 10.1016/j.molcel.2011.12.005. PMID: 22195961; PMCID: PMC3331675. [PubMed]
Jivan, D. (2024). Creatine and cognition. RCSI Research Repository. [Enlace]
Kelly, D.P., & Scarpulla, R.C. (2004). Transcriptional regulatory circuits controlling mitochondrial biogenesis and function. Genes & Development, 18(4), 357–368. [Enlace]
Kim, H. I., Han, Y., & Park, J. (2025). AMP-Activated Protein Kinases in Health and Disease. International Journal of Molecular Sciences, 26(16), 8075. [MDPI]
Latorre-Pellicer, A., et al. (2016). Mitochondrial and nuclear DNA matching shapes metabolism and healthy ageing. Nature, 535(7613), 561–565. [Nature]
Little, J.P., et al. (2011). A practical model of low-volume high-intensity interval training induces mitochondrial biogenesis. J Physiol, 588(6), 1011-1022. [Enlace]
Marshall, R. P., Droste, J.-N., Giessing, J., & Kreider, R. B. (2022). Role of Creatine Supplementation in Conditions Involving Mitochondrial Dysfunction: A Narrative Review. Nutrients, 14(3), 529. https://doi.org/10.3390/nu14030529 [MDPI]
Newman JC, Verdin E. Ketone bodies as signaling metabolites. Trends Endocrinol Metab. 2014 Jan;25(1):42-52. doi: 10.1016/j.tem.2013.09.002. Epub 2013 Oct 18. PMID: 24140022; PMCID: PMC4176946. [PubMed]
Nielsen, F.H. (2010). Magnesium, inflammation, and obesity in chronic disease. Nutr Rev, 68(6), 333–340. [Enlace]
Patti ME, Butte AJ, Crunkhorn S, Cusi K, Berria R, Kashyap S, Miyazaki Y, Kohane I, Costello M, Saccone R, Landaker EJ, Goldfine AB, Mun E, DeFronzo R, Finlayson J, Kahn CR, Mandarino LJ. Coordinated reduction of genes of oxidative metabolism in humans with insulin resistance and diabetes: Potential role of PGC1 and NRF1. Proc Natl Acad Sci U S A. 2003 Jul 8;100(14):8466-71. doi: 10.1073/pnas.1032913100. Epub 2003 Jun 27. PMID: 12832613; PMCID: PMC166252. [PubMed]
Pearson, R. C. et al. (2023). Metabolic response during high-intensity interval exercise and resting vascular and mitochondrial function in CrossFit participants. Kinesiology Journal. [Enlace]
Puigserver, P., & Spiegelman, B.M. (2003). Peroxisome proliferator-activated receptor-γ coactivator 1α (PGC-1α): transcriptional coactivator and metabolic regulator. Endocr Rev, 24(1), 78–90. [Enlace]
Rojas JC, Gonzalez-Lima F. Low-level light therapy of the eye and brain. Eye Brain. 2011 Oct 14;3:49-67. doi: 10.2147/EB.S21391. PMID: 28539775; PMCID: PMC5436183. [PubMed]
Sestili, P. et al. (2016). Cytoprotective effects of creatine in mitochondrial regulation. Amino Acids, 48, 1931–1947.
Snow, W. M., Cadonic, C., & Cortes-Perez, C. (2018). Chronic dietary creatine enhances hippocampal-dependent spatial memory. Learning & Memory, 25(2), 54–60.
Storoschuk, K. L., Moran-MacDonald, A., & Gibala, M. J. (2025). Much Ado About Zone 2: A Narrative Review Assessing the Efficacy of Zone 2 Training for Improving Mitochondrial Capacity and Cardiorespiratory Fitness. Sports Medicine. [Springer]
Taskin, S. et al. (2022). Effects of creatine supplementation on mitochondrial biogenesis. Iranian J. of Basic Medical Sciences, 25(8), 1009–1016. [PubMed]
Theurey, P., & Rieusset, J. (2017). Mitochondria-associated membranes response to nutrient availability and role in metabolic diseases. Trends in Endocrinology and Metabolism, 28(1), 32–45. [Cell]
Türkel İ, Özerkliğ B, Atakan MM, Aktitiz S, Koşar ŞN, Yazgan B. Exercise and Metabolic Health: The Emerging Roles of Novel Exerkines. Curr Protein Pept Sci. 2022;23(7):437-455. doi: 10.2174/1389203723666220629163524. PMID: 35770405. [PubMed]
Wu, Z., et al. (1999). Mechanisms controlling mitochondrial biogenesis and respiration through the thermogenic coactivator PGC-1. Cell, 98(1), 115–124. [Cell]
Valenzuela, A. (2023). Activa tus mitocondrias: El secreto para una vida más longeva. Editorial Planeta.
Yang Z, Luo Y, Yang Z, Liu Z, Li M, Wu X, Chen L, Xin W. Mitochondrial dynamics dysfunction and neurodevelopmental disorders: From pathological mechanisms to clinical translation. Neural Regen Res. 2026 May 1;21(5):1926-1946. doi: 10.4103/NRR.NRR-D-24-01422. Epub 2025 Jun 19. PMID: 40537021; PMCID: PMC12694650. [PubMed]
Zhang, L., Xin, C., Wang, S., Zhuo, S., Zhu, J., Li, Z., & Liu, Y. (2024). Lactate transported by MCT1 plays an active role in promoting mitochondrial biogenesis and enhancing TCA flux in skeletal muscle. Science Advances, 10(45), eadn4508. [Science]

Educador Físico Deportivo. Graduado en Ciencias de la Actividad Física y del Deporte. Colegiado nº 64.218. Máster en Prevención y Readaptación de Lesiones Deportivas en el Fútbol por la UCLM y la RFEF. Máster en Cineantropomería y Nutrición Deportiva por la UV. Técnico Superior en Dietética y Técnico Superior de Fútbol (UEFA Pro). Apasionado del fitness y como deporte futbolero. Tengo la suerte de ayudar a personas a mejorar su salud a través del ejercicio.